Гетерилзамещеные тиазолидоны как перспективная группа противоопухолевых агентов являются объектами углубленных исследований в современной фармацевтической химии. На молекулярном уровне антинеопластические свойства тиазолидонов и родственных гетероциклов связывают с афинитетом к ряду противораковых биомишеней, среди которых энзим JSP-1, фактор ракового некроза TNF, биокомплекс Bcl-XL-BH3 и т.п Кроме того установлено, что 3-замещенные производные 5-арилиден-2-тиоксо-4-тиазолидона ингибируют протеин-тирозин фосфатазы трех типов, а также угнетают рост опухолевых клеток линий Н460 и РС3. Указанные соединения запатентованны как потенциальные средства для лечения и профилактики рака, воспалительных процессов, автоимунных состояний и других нарушений, которые сопровождаются дисрегуляцией клеточного деления и связанные с активностью ферментов протеин-тирозин фосфатаз типов PTPN12 и PTPN2. В последнее время повышается интерес научных работников к гетероциклам с бензтиазольным фрагментом. Так, идентифицировано соединение МКТ 077, которое является зарегистрированным противораковым агентом. Исследование других гетерилзамещенных бензтиазолов также дали возможность выделить ряд перспективных производных.
Проведено исследование 12 производных 5-илиден-2-тиоксо-4-тиазолидону и их 3-бензтиазолиламинозамещенных (Рис. 5).
Противораковую активность синтезированных соединений изучали в Национальном институте рака (США) на 60 линиях клеток, которые охватывают 9 основных групп рака: лейкемию, меланому, рак легких, почек, яичника, ЦНС , толстого кишечника, простаты и молочной железы. Как количественная характеристика использован параметр GР%, что характеризует процент угнетения роста раковых клеток (величина GР% от 100 до 0 %) или их гибели (величина GР% от 0 % к -100 %) при действии исследуемого вещества в концентрации 5 - 10 моль/л.
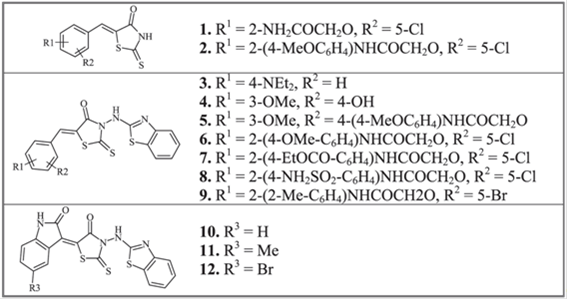
Рис 5. Структура исследованных производных тиазолидона
Следует отметить, что производные 3-(бензтиазол-2-иламино)-2-тиоксо-4-тиазолидона проявляют умеренную противораковую активность с высокой селективностью действия на определенные линии раковых клеток. Так, соединение 4 обнаружило цитостатичний эффект на линию рака почек RXF 393 (GP = -0,71 %), а соединение 9 - на линию HOP-92 (немелкоклеточный рак легких, GP = 0,74 %). Интересно, что введение ацетамидних остатков в арилиденовий фрагмент (в особенности в о-положение) имеет существенное влияние на проявление противораковой активности, о чем свидетельствуют результаты действия соединений 6 и 7 (табл. 1). Так, соединение 7 оказалось эффективным относительно линий лейкемии RPMI-8226 (GP = 20,02 %), MOLT-4 (GP = 36,83 %) и SR (GP = 38,52 %). Высочайшую противораковую активность обнаружило соединение 6, результаты основательного скринингу in vitro которой стали основанием для патентования и углубленных доклиничних исследований иn vivo. Кроме того, заслуживают внимания результаты противораковой активности соединения 12 на такие линии: IGROV1 (рак яичников, GP = 4,59 %), RXF 393 (рак почек, GP = 25,00 %) и SK-MEL-2 (меланома, GP = 25,27 %). Введение атома брома в изатинилиденовий фрагмент (12) оказывает содействие появлению активности, поскольку соединения с остатками изатина (10) или 5-метилизатину (11) не обнаружили такого действия.
На основе изучения противораковой активности производных роданину с бензтиазольним фрагментом идентифицировано «соединение-лидер» 2-{2--4-хлорфенокси}-N-(4-метоксифенил)-ацетамид (6) с высокими показателями ингибирования опухолевого роста без выраженной селективности действия, которое отобрано для углубленного исследования противораковой активности иn vivo.
Выявлено, что наиболее существенное влияние на противораковую активность 3-бензтиазолзамещенних производных роданину имеет размер молекулы и ее разветвленность.