В основе химических методов титриметрии - разнообразные реакции, приводящие к образованию устойчивых продуктов. Классификация методов титриметрии в зависимости от типа используемой реакции приведена в табл. 1.
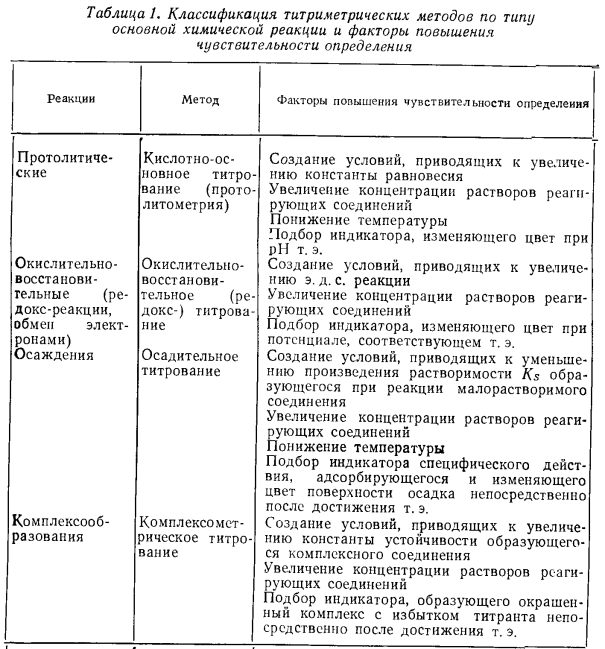
Реакции, используемые для проведения титриметрических определений, должны удовлетворять перечисленным выше требованиям; кроме того, существенное значение имеют устойчивость применяемых стандартных растворов титрантов, условия их хранения, наличие удобного способа стандартизации, информация о стехиометрии и скорости реакции, особенно вблизи точки эквивалентности.
Достоинства метода. Химические методы титриметрии отличаются простотой и точностью, не требуют ни предварительной градуировки, ни дорогостоящего оборудования.
Недостатки метода. Основной источник погрешностей в титриметрии - субъективность восприятия изменения цвета индикатора. В этом случае возможно несоответствие между точкой эквивалентности реакции и фиксацией сигнала индикатора.
Погрешность определений может возникать и вследствие неблагоприятных условий равновесия. Так, при кислотно-основном титровании слабых электролитов затруднен подбор индикатора для реакций с малыми константами равновесия. При проведении редокс-титрований экспериментатор может столкнуться с медленным ходом основной реакции и протеканием побочных взаимодействий, искажающих стехиометрию титрования. В реакциях осаждения могут происходить потери осадка при пептизации или частичном растворении осадка, соосаждении или последующем осаждении примесей. В комплексометрических определениях существенными становятся скорость замещения лигандов и лабильность комплексообразующих частиц.
Условия протекания химических реакций могут быть оптимизированы путем подбора неводных растворителей, вызывающих изменение констант равновесия фармацевтических реакций. Субъективность определения точки эквивалентности устраняют применением физико-химических способов ее фиксации.