Таким образом, уравнение Клайперона примет вид:

Коэффицент i зависит от степени и характера электролитической диссоциации и может быть выражен уравнением:
i=1+α(n+1),
где α - степень электролитической диссоциации,- число элементарных частиц, образующихся из 1 молекулы при диссоциации.
Для разных групп электролитов i может быть подсчитан следующим образом:
А) для бинарных электролитов с однозарядными ионами типа К+А:
α=0,86, n=2;= 1+0,86*(2-1)=1,86
Например, натрия хлорид, калия хлорид, эфедрина гидрохлорид и т.д.
Б) Для бинарных электролитов с двузарядными ионами типа К+²А²:
α=0,5; n=2;
i = 1+0,5*(2-1)=1,5
Например, магния сульфат, атропина сульфат и т.д.
В)Для тринарных электролитов типа К²+А2 и К2 +А²:
α=1; n=3;= 1+1*(3-1)=3
Например, кальция хлорид, натрия гидрофосфат и т.п.
Для изотонирования раствора другим веществом, что встречается очень часто, когда вещества прописаны в небольших количествах и их концентрации недостаточно для изотонирования раствора. При этом расчеты усложняются.
Например: Rp.: Cocaini hydrochloridi 0,1chloride q.s. ut f. sol. isotonici 10 ml.S. Для инъекций по 1 мл.
Рассчитаем его изотоническую концентрацию:
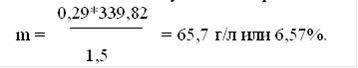
По расчету выписанная концентрация кокаина, значительно ниже, чем необходимая для изотонирования раствора. Определим объем, который изотонирует 0,1 г кокаина.
,57г изотонируют 100 мл раствора, а
,1 г - Х мл раствора.
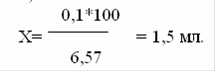
Из этого следует, что натрия хлорида необходимо для изотонирования 10-1,5 = 8,5 мл.
Рассчитаем необходимую массу натрия хлорида:
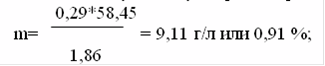
для изотонирования 100 мл раствора надо взять 0,91 г натрия хлорида,
а для изотонирования 8,5 мл - Х г.
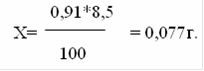
В практической работе расчеты можно упростить путем применения общих формул:
. Если изотоничность достигается одним веществом, для его расчета применяют формулу:

m - количество вещества, добавляемого для изотонирования раствра,- объем изотонируемого раствора (мл),- молекулярная масса вещества,
- число миллилитров.
. Если изотоничность раствора лекарственного вещества достигается с помощью другого (дополнительного) вещества, то применяют формулу:
![]()
![]() - молекулярная масса дополнительного вещества;
- молекулярная масса дополнительного вещества;
![]() - изотонический коэффицент для дополнительного вещества;
- изотонический коэффицент для дополнительного вещества;
![]() - количество дополнительного вещества (г);
- количество дополнительного вещества (г);
![]() ,
, ![]() , i - масса(г), молекулярная масса и изотонический коэффицент для основного вещества.
, i - масса(г), молекулярная масса и изотонический коэффицент для основного вещества.
При более сложных прописях (с тремя и более компонентами) первоначально рассчитывается какой объем раствора изотонируют вещества, чей массы известны. Затем определяется масса изотонирующего компанента. Перейти на страницу: 1 2 3 4 5 6 7 8 9